Análisis de datos públicos
Los datos sobre los linajes del SARS-CoV-2 y la fecha en que se tomó la muestra de las secuencias disponibles en Chile se obtuvieron del sitio Consorcio Genomas CoV2 disponible en https://auspice.cov2.cl/ncov/chile-global. Los datos de vacunación se obtuvieron de datos públicos del Ministerio de Ciencia, Tecnología, Conocimiento e Innovación disponibles en https://github.com/MinCiencia/Datos-COVID19 (Producto 83).
Ensayo de infectividad
Se prepararon virus pseudotipados que portaban diferentes proteínas de pico de SARS-CoV-2 como describimos anteriormente.12. Brevemente, se produjeron pseudotipos de SARS-CoV-1 basados en VIH-2 en células HEK293T transfectando el pNL4.3-ΔEnv-Luc junto con el vector codificante de pico pCDNA-SARS-CoV-2 correspondiente en una proporción molar de 1: 1. Plásmidos que codifican un pico de codón optimizado que carece de los últimos 19 aminoácidos del extremo C-terminal (SΔ19) que se sabe que evitan la retención en el retículo endoplásmico12 se obtuvieron mediante síntesis de genes o mutagénesis dirigida al sitio personalizada (GeneScript) y contenían las siguientes mutaciones: linaje A (secuencia de referencia), linaje B (D614G), linaje B.1.1.7 (Δ69-70, Δ144, N501Y, A570D, D614G, P681H, T716I, S982A, D1118H), linaje P.1 (L18F, T20N, P26S, D138Y, R190S, K417T, E484K, N501Y, D614G, H655Y, T1027I) y linaje C.37 (G75V, T76I) 246, L252Q, F452S, D490G, T614N). Cada preparación de pseudotipo se eliminó mediante centrifugación a 859 rpm a temperatura ambiente, se cuantificó utilizando el kit ELISA HIV-3,000 Gag p1 Quantikine (R&D Systems), se dividió en alícuotas en suero bovino fetal al 24% (Sigma-Aldrich) y se almacenó a -50 ° C hasta utilizar. Se usaron diferentes cantidades de virus pseudotipados (determinados por los niveles de la proteína p80 del VIH-1) para infectar células HEK-ACE24 y, 2 horas después, se midió la actividad de luciferasa de luciérnaga usando el reactivo de ensayo de luciferasa (Promega) en una microplaca Glomax 48 luminómetro (Promega).
Ensayo de neutralización
Los ensayos de neutralización de virus pseudotipados se realizaron esencialmente como describimos anteriormente.12. Brevemente, se prepararon diluciones seriadas de las muestras de plasma (1: 4 a 1: 8748) en DMEM con suero fetal bovino al 10% y se incubaron con 5 ng de p24 de cada virus pseudotipado durante 1h a 37 ° C y luego, 1 × 104 de células HEK-ACE2 se añadieron a cada pocillo. Las células HEK293T (que no expresan ACE2) incubadas con el virus pseudotipado (linaje A) se utilizaron como control negativo. Las células se lisaron 48 horas después y se midió la actividad de luciferasa de luciérnaga usando el reactivo de ensayo de luciferasa (Promega) en un luminómetro de microplacas Glomax 96 (Promega). Se calculó el porcentaje de neutralización para cada dilución y se calculó el ID50 de cada muestra utilizando GraphPad Prism versión 9.0.1.
Análisis estadístico
Los análisis estadísticos se realizaron utilizando el software GraphPad Prism versión 9.1.2. Se llevaron a cabo comparaciones de múltiples grupos para los títulos de anticuerpos neutralizantes (NAbT) contra un panel de virus pseudotipados del SARS-CoV-2, así como las comparaciones de las respuestas de NAbs por sexo y estado de humo utilizando una prueba emparejada de Wilcoxon con signo y clasificación. El cambio de factor se calculó como la diferencia del título medio geométrico en el ID50 en comparación con el del virus pseudotipado de tipo salvaje. El análisis de correlación entre NAbT y la edad o el IMC se realizó mediante la prueba de Spearman. Se realizaron ANOVA de una vía y la prueba de comparación múltiple de Tukey para el análisis estadístico de la infectividad. Se consideró estadísticamente significativo un valor de p ≤ 0.05.
Aprobación ética
El protocolo de estudio fue aprobado por el Comité de Ética de la Facultad de Medicina de la Universidad de Chile (Proyectos N ° 0361-2021 y N ° 096-2020) y Clínica Santa María (Proyecto N ° 132604-21). Todos los donantes firmaron el consentimiento informado y sus muestras se anonimizaron.
Impacto de las mutaciones de pico en la variante Lambda sobre la infectividad y las respuestas de anticuerpos neutralizantes
Un análisis de 3695 secuencias de Chile depositadas en GISAID al 24 de junioth 2021 muestra un claro predominio de las variantes Gamma y Lambda del SARS-CoV-2 durante el último trimestre que, juntas, representan el 79% de todas las secuencias.
Curiosamente, este período se ha caracterizado por una campaña de vacunación masiva en la que el 65.6% de la población objetivo (personas de 18 años y mayores) ha recibido un esquema de vacunación completo al 27 de junio.th 2021
Dado que el 78.2% de las personas inoculadas con un esquema completo recibieron la vacuna de virus inactivado CoronaVac de Sinovac Biotech, buscamos investigar el impacto de las mutaciones de pico presentes en la variante Lambda sobre la capacidad neutralizante de los anticuerpos provocados por esta vacuna.
Para ello, generamos virus pseudotipados SARS-CoV-1 basados en el VIH-2 que llevan la proteína de pico del linaje de referencia Wuhan-1 (tipo salvaje; linaje A), la mutación D614G (linaje B) y el alfa (linaje B) .1.1.7), variantes Gamma (linaje P.1) y Lambda (linaje C.37).
Durante la preparación del virus, observamos consistentemente que las células infectadas con el virus pseudotipado que lleva el pico Lambda produjeron valores de bioluminiscencia significativamente más altos en comparación con el mutante D614G o las variantes Alfa y Gamma, lo que indica una mayor infectividad impulsada por la proteína pico Lambda.

Figura 1.Infectividad mediada por diferentes proteínas de pico.
(A) Representación esquemática de la proteína de pico de SARS-CoV-2 y las variantes utilizadas en este estudio. Los linajes se indican entre paréntesis. RBD, dominio de unión al receptor, CM; cola citoplasmática.
(B) Titulación de los pseudotipos de cada linaje utilizando cantidades equivalentes de p1 del VIH-24. La actividad luciferasa de luciérnaga se midió como unidades de luminiscencia relativa (RLU) a las 48 horas después de la infección. El promedio y la DE se calcularon a partir de un experimento por triplicado representativo.
A continuación, utilizamos los virus pseudotipados mencionados anteriormente para realizar ensayos de neutralización utilizando 79 muestras de plasma de trabajadores sanos de la salud de la Universidad de Chile y Clínica Santa María en Santiago, Chile.
Excluimos 4 muestras porque no pudimos calcular un título de ID50. De las muestras analizadas, el 73% correspondió a mujeres, mediana de edad 34 años (IQR 29 - 43) y un índice corporal máximo (IMC) de 25 (IQR 22.7 - 27). Un 20.5% de los participantes declaró ser fumador activo mientras duró el período de vacunación. Las muestras se obtuvieron en una mediana de 95 días (IQR 76 - 96) después de la segunda dosis de la vacuna CoronaVac.
Observamos que la neutralización del virus pseudotipado que lleva la proteína de pico de tipo salvaje resultó en una dilución inhibidora del 50% (ID50) título medio de 191.46 (154.9 - 227.95, IC del 95%,), mientras que fue 153.92 (115.68 - 192.16, IC del 95%), 124.73 (86.2 - 163.2, IC del 95%), 104.57 (75.02 - 134.11, IC del 95% ) y 78.75 (49.8 - 107.6, IC del 95%) para los virus pseudotipados que llevan la proteína de pico del mutante D614G o las variantes Alfa, Gamma y Lambda, respectivamente.
También observamos que la media geométrica del título de la DI50 los títulos disminuyeron en un factor de 3.05 (2.57 - 3.61, IC del 95%) para el virus pseudotipado que porta el pico Lambda, 2.33 (1.95 - 2.80, IC del 95%) para el pico Gamma, 2.03 (1.71 - 2.41, IC del 95%) para el pico Alpha y 1.37 (1.20 - 1.55, IC del 95%) para el pico D614G en comparación con el pico de tipo salvaje.
En nuestra cohorte de estudio no se observó ninguna correlación entre el sexo, la edad, el índice de masa corporal (IMC) o el estado del tabaquismo y los títulos de anticuerpos neutralizantes.
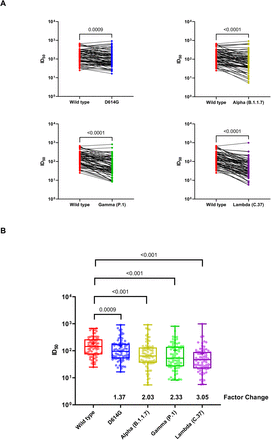
Figura 2.Ensayo de neutralización utilizando muestras de plasma de vacunados CoronaVac
(A) Cambios en el título de neutralización recíproco al 50% (ID50) en muestras de plasma de 75 receptores de la vacuna CoronaVac contra D614G (linaje B), Alpha (linaje B.1.1.7),
Variantes Gamma (linaje P.1) y Lambda (linaje C.37) en comparación con el virus de tipo salvaje. Los resultados se muestran como la diferencia en los títulos de neutralización de muestras emparejadas. Valores de p para la comparación de la ID50 se calculan con la prueba de rango con signo de Wilcoxon.
(B) Los diagramas de caja indicaron la mediana y el rango intercuartílico (IQR) de ID50 para cada virus pseudotipado. Los cambios de factor se muestran como la diferencia del título medio geométrico en el ID50 en comparación con los del virus pseudotipado de tipo salvaje. Los análisis estadísticos se realizaron utilizando la prueba de rango con signo de pares emparejados de Wilcoxon.
Juntos, nuestros datos revelaron que la proteína de pico de la variante de interés recientemente reconocida Lambda, que circula mucho en Chile y los países de América del Sur, porta mutaciones que confieren una mayor infectividad y la capacidad de escapar de los anticuerpos neutralizantes provocados por CoronaVac.






















